Transition De L'emballage Médical Tyvek®
Projet de transition d'emballage médical (PTEM) DuPont™ Tyvek®
DuPont passe Tyvek® 1073B et Tyvek® 1059B vers des lignes de production intégrant la technologie la plus récente en matière de filage éclair afin d'améliorer la continuité et la flexibilité de l'offre future.
Le projet de transition d'emballage médical DuPont™ Tyvek®, connu sous le sigle PTEM, comprend une méthode systématique de génération de données qui prouve que les performances de Tyvek®, produit sur les nouvelles lignes, sont fonctionnellement équivalentes à celles de Tyvek® que vous achetez actuellement. Tout est fait dans l'objectif de limiter la requalification réglementaire et réduire les coûts pour les sociétés individuelles de ce marché. L'équivalence fonctionnelle signifie que l'attribut que vous mesurez pourra être différent, même sur le plan statistique, mais qu'il continuera à satisfaire les exigences en termes de fonctionnement et de performances, afin que vos processus et applications bénéficient de performances identiques à celles de Tyvek® actuel.
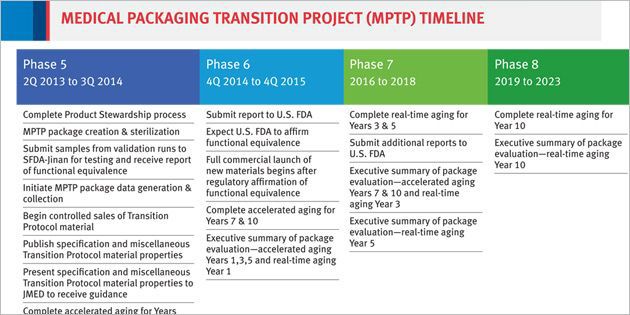
Calendrier du PTEM
Trois éléments d'étude
Le projet de transition d'emballage médical Tyvek® est composé de trois éléments d'étude :
- le protocole de transition de la FDA aux États-Unis (le « protocole de transition ») : un programme d'étude qui implique la production d'emballages de dispositifs médicaux stérilisés, ainsi que leurs essais. Ces emballages ont été passés en revue et acceptés par le CDRH (Center for Devices and Radiological Health) de la FDA aux États-Unis.
- le protocole fantôme : essais supplémentaires réalisés sur les applications et les technologies qui n'entrent pas dans le champ d'application du protocole de transition mais qui ont été demandés par l'Industrie pour prendre en charge l'évaluation des risques.
- Gestion responsable des produits : chaque produit DuPont commercialisé nécessite une étude formelle de gestion responsable des produits afin d'en évaluer les risques et leur aptitude à l'emploi.
PTEM : une priorité absolue pour DuPont
DuPont réalise un investissement pluriannuel de plus de 30 millions de dollars et dispose d'une équipe multifonctionnelle et internationale impliquée dans le projet de transition d'emballage médical DuPont™ Tyvek® afin que cette transition se réalise en douceur pour les fabricants d'emballages stériles, les fabricants de dispositifs médicaux, et les différents acteurs du secteur de santé. L'investissement de DuPont couvre :
- le soutien à l'Industrie et aux réglementations mondiales
- les matières premières pour les lignes multiples et les essais sur les polymères
- la création et les tests sur les emballages expérimentaux
- la création et les tests sur les emballages du protocole de transition
- les essais dans les laboratoires tiers
- le protocole fantôme
- la gestion responsable des produits
Initiative collaborative
Le projet de transition d'emballage médical DuPont™ Tyvek® est le fruit de la collaboration entre les fabricants d'emballages stériles, les fabricants de dispositifs médicaux, les organismes de réglementation, les laboratoires d'essais et les entreprises de stérilisation sous contrat du monde entier. Le projet de transition d'emballage médical DuPont™ Tyvek® ne serait pas possible sans la collaboration de l'Industrie.
Documents d’orientation réglementaire et données relatives au PTEM
Pour assister les fabricants de dispositifs médicaux dans leur évaluation des risques, nous publions les données issues du projet de transition d'emballage médical DuPont™ Tyvek® dès qu'elles sont disponibles. Outre ces données, nous publions les conseils obtenus auprès des organismes de réglementation du monde entier, dans le but d'informer les fabricants de dispositifs médicaux.
Les données du Projet de transition d'emballage médical Tyvek®, prouvant l'équivalence fonctionnelle ainsi que les documents réglementaires explicatifs provenant des autorités du monde entier, sont disponibles au téléchargement. Les nouvelles données techniques sont ajoutées dès leur disponibilité.
Des membres importants de l'équipe partagent quelques exemples de progrès significatifs, réalisés depuis l'annonce du projet en juin 2011, et discutent de l'expansion du champ d'application du projet pour y inclure des essais supplémentaires, requis par le secteur dans le cadre de l'évaluation des risques.